2025年10月22日
機能性表示食品制度の改正のポイントと対応策 ~新告示・GMPの義務化と容器包装の在り方の見直しについて~

特別寄稿
消費者庁 食品表示課 保健表示室
昨年9月より健康被害情報の報告義務化などが施行され、来年にはGMP基準の対応・パッケージ表示の見直しが予定されている『機能性表示食品制度』については、JADMAでも7月に関連するセミナーを開催するなど、改めて関連事業者に向けた周知を行っている。
今号では、消費者庁・食品表示課保健表示室より、GMPの義務化と容器包装の在り方の見直しなど新告示について解説いただいた。
1.はじめに
令和6年3月に、小林製薬㈱の紅麹関連製品について健康被害の発生が報告された。消費者庁としては、同年5月31日に開催された「紅麹関連製品への対応に関する関係閣僚会合」における取りまとめを踏まえ、機能性表示食品制度の見直しを行った(図表1)。以下、詳細について説明する。

2.小林製薬の紅麹関連製品による健康被害を踏まえた対応
関係閣僚会合の取りまとめでは、今回の事案を踏まえた今後の対応として、①健康被害の情報提供の義務化、②機能性表示食品制度の信頼性を高めるための措置、③情報提供のDX化、消費者教育の強化、④国と地方の役割分担について記載されている。
以上を踏まえ、令和6年9月1日及び令和7年4月1日に食品表示基準及び告示について公布された。
今回の制度の見直し項目は大きく分けて4点である(図表2)。
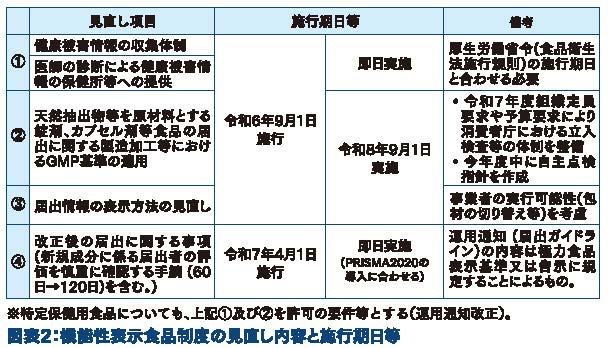
(1)健康被害の情報収集体制を整えて、医師の診断による健康被害情報があった場合には、保健所等への提供を行うこと
健康被害情報の提供については、令和6年9月1日から経過措置期間を設けず施行しており、既に届出者の皆様にご対応いただいているところである。
(2)天然抽出物等を原材料とする錠剤、カプセル剤等食品を製造・加工する場合にはGMP基準を適用すること
機能性表示食品のうち、天然抽出物等を原材料とする錠剤、カプセル剤等食品については、「機能性表示食品のうち天然抽出物等を原材料とする錠剤、カプセル剤等食品の製造又は加工の基準」に基づく管理が必要となる。
原材料を受け入れて、天然抽出物等を原材料とする錠剤、カプセル剤等食品を製造する施設が、そのまま製品をパッケージして製品として販売する場合、当該施設のみがGMP基準に基づく管理を行うこととなる。例えば、天然抽出物等を原材料とする錠剤やカプセル剤等食品を製造する施設を製造所A、製造された当該食品を大きな袋などに入れて製造所Aから運搬し、小分け包装する施設を加工所Bとした場合、加工所Bにおいて運搬された当該食品そのものに手で触れることができるなどの衛生状態の変更が行われる場合にあっては、加工所BにおいてもGMP基準に基づく管理が必要となる。この例の場合、小分け包装された製品を更に化粧箱等に梱包するための施設に持っていくことなども想定されるが、製品を直接手で触れるなどの操作が生じず、衛生状態の変更がないのであれば、当該施設はGMP基準に基づく管理は必要ないということになる。
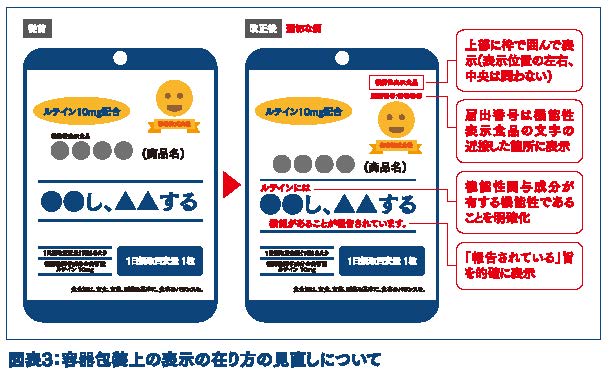
(3)届出情報の表示方法の見直し(図表3)
①「機能性表示食品」の表示位置
「機能性表示食品」という文言はこれまでも容器包装の主要面に表示することとなっていたが、今後は「主要面の上部に」、「枠で囲んで」という二つの条件が新たに加わるとともに、届出番号は機能性表示食品である旨の表示に近接した箇所、つまり主要面の上部に表示をする必要がある。
②科学的根拠を有する機能性関与成分及び当該成分又は当該成分を含有する食品が有する機能性
これまでの「届出表示」から「機能性表示」と冠することを食品表示基準に規定した。また、同基準において、表示の方法は「機能性関与成分が有する機能性を表示する場合」と、「機能性関与成分を含有する食品が有する機能性を表示する場合」とを分けて規定している。
なお、機能性表示食品の届出の多くが「機能性関与成分が有する機能性を表示する場合」に該当し、その食品そのもので臨床試験(ヒト試験)をして届出しているわけではない。その場合、届出された食品そのものに機能があるかのように消費者に誤認させてはならないという観点で、機能性関与成分が有する機能性について「報告されている旨」を的確に示す文言として表示をする必要がある。
一方、「機能性関与成分を含有する食品が有する機能性」を表示する場合(=届出する食品そのもので行った臨床試験(ヒト試験)を基に届出する場合)、機能性表示食品制度はあくまでも「機能性関与成分」に着目した制度であるため、機能性関与成分が入っているので結果的に食品に機能がある、という趣旨の表示をする必要がある。
③機能性及び安全性について、国による評価を受けたものではない旨
これまでとは異なり「本品は、特定保健用食品と異なり、機能性及び安全性について国による評価を受けたものではありません。届け出られた科学的根拠等の情報は消費者庁のウェブサイトで確認できます。」という表示に改正した。本制度はウェブサイトで確認できるということが大切な制度であるため、新たにウェブサイトで確認できる旨も表示をする必要がある。
④摂取をする上での注意事項
より具体的に、「医薬品及び他の機能性関与成分との相互作用、過剰摂取等に係る注意喚起等について、当該機能性関与成分の安全性に関する科学的根拠を踏まえて具体的に表示する。」と規定した。
⑤疾病の診断、治療、予防を目的としたものではない旨
「医薬品と異なり、疾病の診断、治療、予防を目的としたものではない旨又は医薬品ではない旨を表示する。」という表示に改正した。
定型の文章ではなく、「医薬品と異なり、疾病の診断、治療、予防を目的としたものではない旨又は医薬品ではない旨」としているため、例えば「医薬品ではありません。」とだけ表示することでも差し支えない。
⑥疾病に罹患している者は医師、医薬品を服用している者は医師、薬剤師に相談した上で摂取すべき旨
「疾病に罹患している者は医師に、医薬品を服用している者は医師、薬剤師に摂取について相談すべき旨を表示する。」という表示に改正した。医師等に何を相談するかを明確にするため、「摂取について相談すべき旨」という文言を追加している。
⑦その他
容器包装に消費者にわかりやすい情報を提供する等の目的で、機能性表示の内容を一部省略、簡素化・言い換え・追加説明等をする場合には、機能性表示の内容が著しく強調・誤認されることのないようにフォントサイズ、配色、背景色等に留意が必要である。
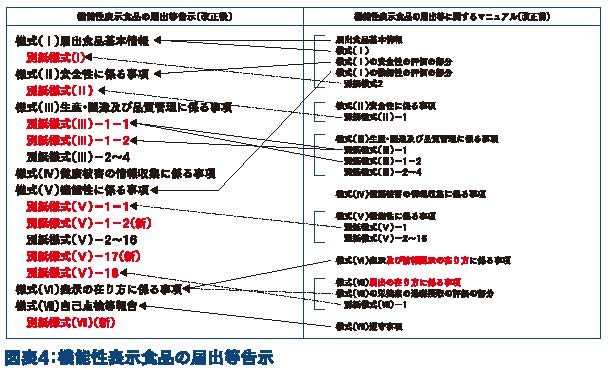
(4)機能性表示食品の届出等告示
機能性表示食品の届出等告示は、条文、様式、別紙様式及び記載要領で構成し、様式及び別紙様式については、届出ガイドラインを廃止し発出していた「機能性表示食品の届出等に関するマニュアル」と原則同様の内容を規定している(図表4)。
記載要領については、原則、届出マニュアルに記載されていた内容に沿って、様式等に具体的に何を記載するかを示した。また、PRISMA声明2020へ準拠することや、年1回の遵守事項の自己点検に関するチェックリストを規定している。
届出にあたって、告示に規定されている様式等については、法令に位置づけられている様式となるため、原則改変不可となること、また令和7年4月1日から必須となったため、届出にあたっては、これらの点についても注意する必要がある。
(5)機能性表示食品制度届出データベース等の更改
令和7年4月1日に食品関連事業者が機能性表示食品の届出を行うためのシステムである「機能性表示食品制度届出データベース」及び機能性表示食品の届出情報を閲覧するための「機能性表示食品の届出情報検索」を更改した。この更改により、「機能性表示食品の届出情報検索」では、PRISMA声明2020の準拠の届出一覧での確認や、スマートフォンに対応した表示が可能となる等、検索機能の強化を行った。
(欄外)
※図表については消費者庁HP「機能性表示食品制度に関する説明会(https://www.caa.go.jp/notice/entry/040995/)」よりご確認いただけます。
【関連記事】